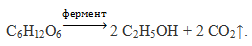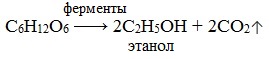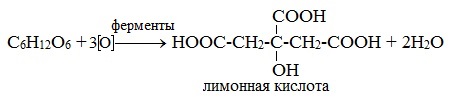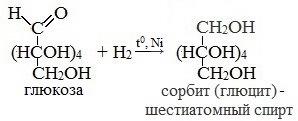Глюкоза
Характеристики и физические свойства глюкозы
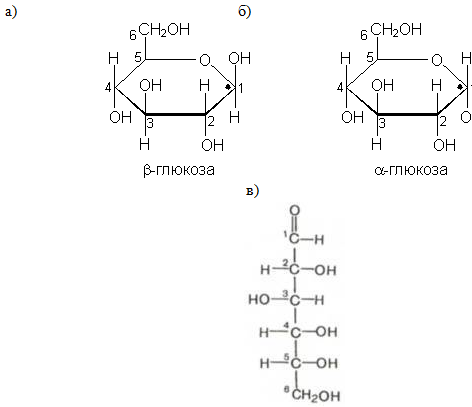
Молекулы глюкозы могут существовать в линейной (альдегидоспирт с пятью гидроксильными группами) и циклической форме (α- и β-глюкоза), причем вторая форма получается из первой при взаимодействии гидроксильной группы при 5-м атоме углерода с карбонильной группой (рис. 1).
Рис. 1. Формы существования глюкозы: а) β-глюкоза; б) α-глюкоза; в) линейная форма
Получение глюкозы
В промышленности глюкозу получают гидролизом полисахаридов – крахмала и целлюлозы:
Химические свойства глюкозы
Для глюкозы характерны следующие химические свойства:
1) Реакции, протекающие при участии карбонильной группы:
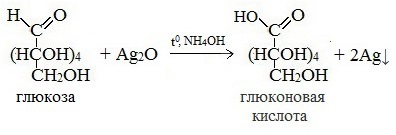
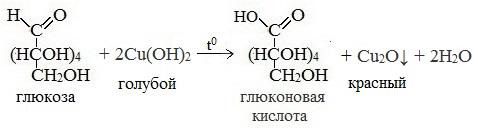
— глюкоза окисляется аммиачным раствором оксида серебра (1) и гидроксидом меди (II) (2) в глюконовую кислоту при нагревании
— глюкоза способна восстанавливаться в шестиатомный спирт – сорбит
— глюкоза не вступает в некоторые реакции, характерные для альдегидов, например, в реакцию с гидросульфитом натрия.
2) Реакции, протекающие при участии гидроксильных групп:
— глюкоза дает синее окрашивание с гидроксидом меди (II) (качественная реакция на многоатомные спирты);
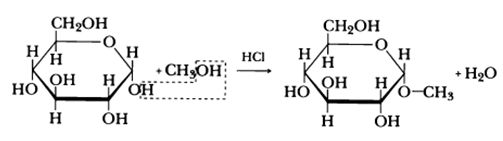
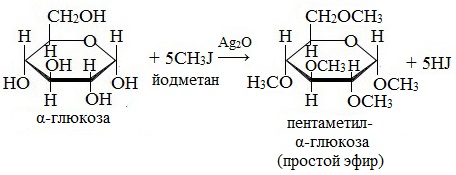
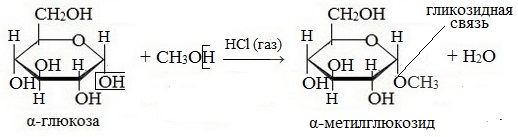
— образование простых эфиров. При действии метилового спирта на один из атомов водорода замещается на группу СН3. В эту реакцию вступает гликозидный гидроксил, находящийся при первом атоме углерода в циклической форме глюкозы
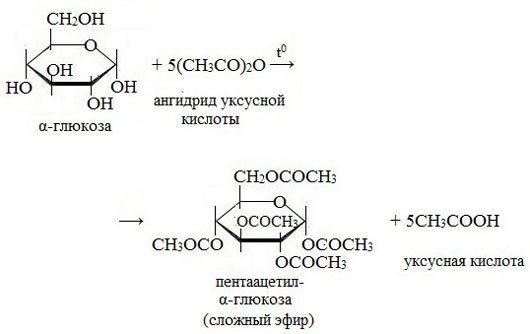
— образование сложных эфиров. Под действием уксусного ангидрида все пять групп –ОН в молекуле глюкозы замещаются на группу –О-СО-СН3.
Применение глюкозы
Глюкоза находит широкое применение в текстильной промышленности при крашении и печатании рисунков; изготовлении зеркал и елочных украшений; в пищевой промышленности; в микробиологической промышленности как питательная среда для получения кормовых дрожжей; в медицине при самых разнообразных заболеваниях, особенно при истощении организма.
Примеры решения задач
| Задание | Составьте уравнения реакций между глюкозой и следующими веществами: а) водородом (в присутствии катализатора); б) азотной кислотой; в) аммиачным раствором оксида серебра. При каких условиях протекают эти реакции? |
| Ответ | При взаимодействии глюкозы с водородом в присутствии катализатора (обычно никель) и при нагревании происходит её восстановление. Продуктом этой реакции является шестиатомный спирт – сорбит, который применяется в качестве заменителя сахара: |
Качественной реакцией на альдегидную группу является реакция «серебряного зеркала» (глюкоза представляет собой альдегидоспирт) в результате чего выделяется серебро в чистом виде и образуется карбоновая кислота:
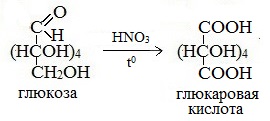
Окисление глюкозы в жестких условиях, например, концентрированной азотной кислотой, приводит к образованию глюкаровой кислоты:
| Задание | Рассчитайте объем оксида углерода (IV), приведенный к нормальным условиям, который выделится при спиртовом брожении 225 г глюкозы. |
| Решение | Запишем уравнение реакции спиртового брожения глюкозы: |
Рассчитаем количество вещества глюкозы:
M(C6H12O6) = 2×Ar(C) + 12×Ar(H) + 6×Ar(O) = 2×12 + 12×1 + 6×16 = 180г/моль;
Согласно уравнению реакции n(C6H12O6) : n(CO2) = 1 : 2, значит
Найдем объем выделившегося углекислого газа:
Источник статьи: http://ru.solverbook.com/spravochnik/ximiya/soedineniya/glyukoza/
Процессы антонимы характерные для глюкозы
Химические свойства глюкозы, как и других альдоз, обусловлены присутствием в ее молекуле: а)альдегидной группы; б) спиртовых гидроксилов; в) полуацетального (гликозидного) гидроксила.
Специфические свойства
1. Брожение (ферментация) моносахаридов
Важнейшим свойством моносахаридов является их ферментативное брожение, т.е. распад молекул на осколки под действием различных ферментов. Брожению подвергаются в основном гексозы в присутствии ферментов, выделяемых дрожжевыми грибками, бактериями или плесневыми грибками. В зависимости от природы действующего фермента различают реакции следующих видов:
1) Спиртовое брожение
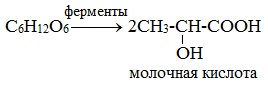
2) Молочнокислое брожение
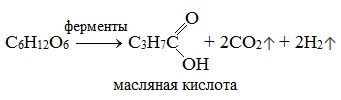
3) Маслянокислое брожение
4) Лимоннокислое брожение
Реакции с участием альдегидной группы глюкозы (свойства глюкозы как альдегида)
1. Восстановление (гидрирование) с образованием многоатомного спирта
В ходе этой реакции карбонильная группа восстанавливается и образуется новая спиртовая группа:
Cорбит содержится во многих ягодах и фруктах, особенно много сорбита в плодах рябины.
2. Окисление
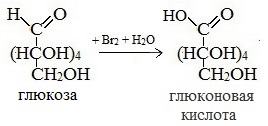
1) Окисление бромной водой
Качественные реакции на глюкозу как альдегид!
Протекающие в щелочной среде при нагревании реакции с аммиачным раствором Ag2O (реакция серебряного зеркала») и с гидроксидом меди (II) Cu (OH)2 приводят к образованию смеси продуктов окисления глюкозы.
2) Реакция серебряного зеркала
Соль этой кислоты – глюконат кальция – известное лекарственное средство.
Видеоопыт «Качественная реакция глюкозы с аммиачным раствором оксида серебра (I)»
3) Окисление гидроксидом меди (II)
В ходе этих реакций альдегидная группа – СНО окисляется до карбоксильной группы – СООН.
Реакции глюкозы с участием гидроксильных групп (свойства глюкозы как многоатомного спирта)
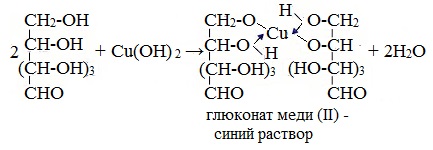
1. Взаимодействие с Cu (ОН)2 с образованием глюконата меди (II)
Качественная реакция на глюкозу как многоатомный спирт!
Подобно этиленгликолю и глицерину, глюкоза способна растворять гидроксид меди (II), образуя растворимое комплексное соединение синего цвета:
Прильём к раствору глюкозы несколько капель раствора сульфата меди (II) и раствор щелочи. Осадка гидроксида меди не образуется. Раствор окрашивается в ярко-синий цвет.
В данном случае глюкоза растворяет гидроксид меди (II) и ведет себя как многоатомный спирт, образуя комплексное соединение.
Видеоопыт «Качественная реакция глюкозы с гидроксидом меди (II)»
2. Взаимодействие с галогеналканами с образованием простых эфиров
Являясь многоатомным спиртом, глюкоза образует простые эфиры:
Реакция происходит в присутствии Ag2O для связывания выделяющегося при реакции НI.
3. Взаимодействие с карбоновыми кислотами или их ангидридами с образованием сложных эфиров.
Например, с ангидридом уксусной кислоты:
Реакции с участием полуацетального гидроксила
1. Взаимодействие со спиртами с образованием гликозидов
Гликозиды – это производные углеводов, у которых гликозидный гидроксил замещен на остаток какого-либо органического соединения.
Содержащийся в циклических формах глюкозы полуацетальный (гликозидный) гидроксил является очень реакционноспособным и легко замещается на остатки различных органических соединений.
В случае глюкозы гликозиды называются глюкозидами. Связь между углеводным остатком и остатком другого компонента называется гликозидной.
Гликозиды построены по типу простых эфиров.
При действии метилового спирта в присутствии газообразного хлористого водорода атом водорода гликозидного гидроксила замещается на метильную группу:
В данных условиях в реакцию вступает только гликозидный гидроксил, спиртовые гидроксильные группы в реакции не участвуют.
Гликозиды играют чрезвычайно важную роль в растительном и животном мире. Существует огромное число природных гликозидов, в молекулах которых с атомом С (1) глюкозы остатки самых различных соединений.
Реакции окисления
Более сильный окислитель – азотная кислота НNO3 – окисляет глюкозу до двухосновной глюкаровой (сахарной) кислоты:
В ходе этой реакции и альдегидная группа – СНО и первичная спиртовая группа — СН2ОН окисляются до карбоксильных – СООН.
Видеоопыт «Окисление глюкозы кислородом воздуха в присутствии метеленового голубого»
Источник статьи: http://himija-online.ru/organicheskaya-ximiya/uglevody/ximicheskie-svojstva-glyukozy.html