Что такое Озон?
Начнем с самого простого вопроса: Откуда вообще берется озон и что это такое?
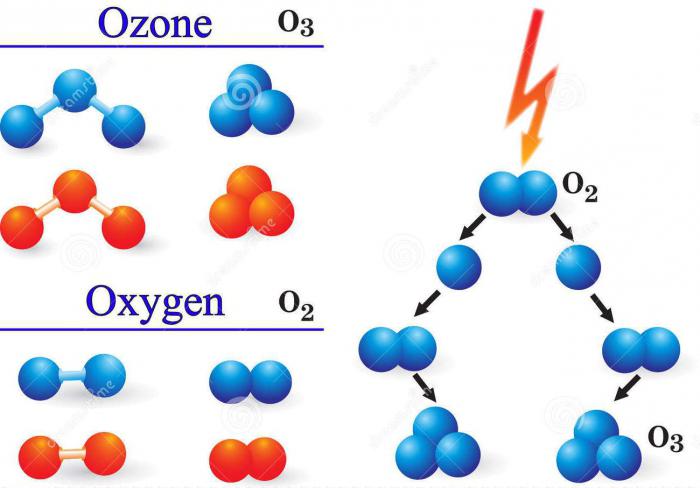
Для того, чтобы нам с вами жить, нужен кислород, то есть молекулы О2. Об этом все мы знаем еще со школы. Однако, кислород имеет аллотропную модификацию: О3, которую называют озоном.
В природе озон может образоваться несколькими способами. Первый – благодаря солнечной радиации. Второй – благодаря электрическим разрядам в атмосфере, то есть молниям.
Третий – в электромагнитных полях силовых кабелей и других электрических устройств.
Какое применение имеет озон?
Во-первых , озон является хорошим средством для обеззараживания питьевой воды, очистки промышленных сточных вод и выбросов в атмосферу от вредных примесей, например от фенолов и цианидов.
Во-вторых , в химии озон применяется как сильный окислитель.
Благодаря этому свойству озон используется для стерилизации изделий медицинского назначения; для отбеливания бумаги; для очистки масел.
Так что озон можно считать санитаром окружающей среды.
Также, тот факт, что озон более сильный окислитель, чем кислород нашел применение озону в качестве окислителя ракетного топлива. Только не в чистом виде, а в виде смеси кислород-озон.
В чистом виде жидкий озон не применяют, так как он химически неустойчив и взрывоопасен. Да к тому же озон еще и токсичен. На этом моменте плавно перейдем к отрицательным моментам, связанным с озоном.
Как выясняется, озон не во всех случаях полезен.
Конечно в XXI веке многие фирмы выпускают бытовые озонаторы для дезинфекции помещений, например для дома. Но почему-то они умалчивают о мерах безопасности.
Когда вы обеззараживаете помещение, используя такой прибор, не надо самому при этом присутствовать в помещении. Иначе вы рискуете медленно, но верно обеззаразить помещение и от себя, так как озон токсичен.
А потом кругом кричат, что экология у нас дрянь, сосед умер от рака, А ведь не пил, не курил, озонатором пользовался, за здоровьем следил.
Да, существуют озонотерапии в некоторых медицинских учреждениях. Но их эффективность клинически не доказана и в развитых странах озонотерапия не признаётся лекарственным методом.
Но если вы хотите дома убить плесень и бактерии, то озон к вашим услугам.
Что еще может сделать озон. Ну например…, хотя возле земли его мало, но его достаточно, чтобы разрушать резину, да хотя бы покрышек автомобилей или в рамах пластиковых окон. Резина трескается и постепенно разрушается.
На высоте 20-25 км над землей находится так называемый озоновый слой. В нем наибольшее содержание озона, где он образуется в результате воздействия ультрафиолетового излучения Солнца на молекулу кислорода.
Ультрафиолетовое излучение также действует на озон, разрушая его. При этом почти полностью поглощается жесткая часть ультрафиолета, которая вызывает загар и рак кожи, и до поверхности Земли доходит лишь несколько процентов.
Озоновый слой образовался в атмосфере Земли примерно 500—600 млн лет назад, когда в ней накопилось достаточно кислорода вследствие фотосинтеза. И только лишь после образования озонового слоя жизнь смогла выйти из океанов;
Без этого высокоразвитые формы жизни типа млекопитающих, включая человека, не возникли бы.
Теперь поговорим о химическом получении озона.
Для этого используем реакцию персульфата аммония с азотной кислотой:
3 (NH4)2S2O8 + 6 HNO3 + 3 H2O = 6 NH4NO3 + 6 H2SO4 + O3
Осторожно подогреем смесь в колбочке и пропустим выходящий газ через раствор иодида калия. В результате образуется йод и раствор окрашивается в жёлтый цвет:
2 KI + O3 + H2O = 2 KOH + I2 + O2
Подводя итоги можно сказать о том, что озон является как помощником человека в некоторых делах и спасителем от солнечной радиации, так и сильным окислителем и ядовитым газом, который оказывает очень пагубное влияние.
Источник статьи: http://zen.yandex.ru/media/chemistryeasy/chto-takoe-ozon-5c70682c13cc4400b3abd275
Озон (химический элемент): свойства, формула, обозначение
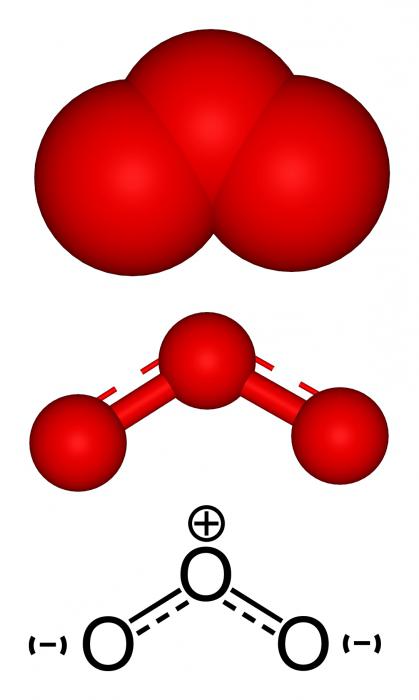
Крайне ценными для всего человечества свойствами обладает такой газ, как озон. Химический элемент, которым он образован, — это кислород О. На самом деле, озон О3 – одна из аллотропных модификаций оксигена, состоящая из трёх формульных единиц (О÷О÷О). Первое и более известное соединение – это сам кислород, точнее газ, который образован двумя его атомами (О=О) – О2.
Аллотропия – это способность одного химического элемента образовывать ряд различных по свойствам простых соединений. Благодаря ей человечество изучило и использует такие вещества, как алмаз и графит, моноклинная и ромбическая сера, кислород и озон. Химический элемент, имеющий такую способность, не обязательно ограничен только двумя модификациями, у некоторых их больше.
История открытия соединения
Составляющая единица многих органических и минеральных веществ, в том числе и такого как озон – химический элемент, обозначение которого О – оксиген, в переводе с греческого «oxys» — кислый, и «gignomai» — рождать.
Впервые новую аллотропную модификацию кислорода во время опытов с электрическими разрядами обнаружил в 1785 году голландец Мартин ван Марун, его внимание привлёк специфический запах. А веком позже француз Шенбейн отметил присутствие такого же после грозы, в результате чего газ был назван «пахнущий». Но учёные несколько обманулись, считая, что их обоняние учуяло сам озон. Запах, который они чувствовали, принадлежал органическим соединениям, окисленным при взаимодействии с О3, так как газ очень реакционноспособен.
Электронное строение
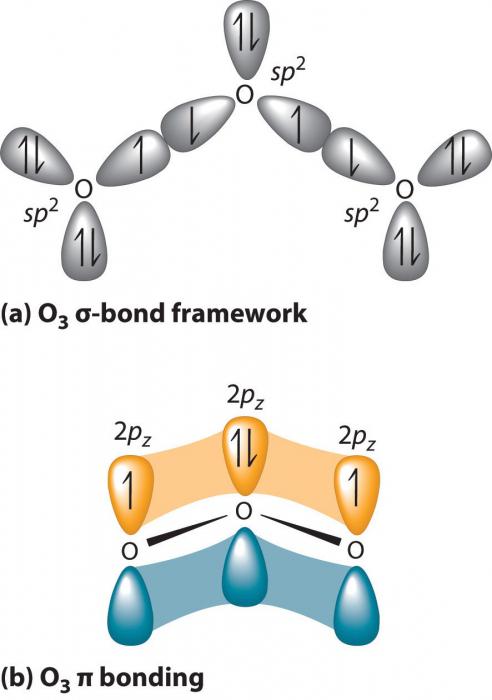
Один и тот же структурный фрагмент имеют О2 и О3 – химический элемент. Озон имеет более сложное строение. В кислороде же всё просто – два атома оксигена соединены двойной связью, состоящей из ϭ- и π-составляющей, согласно валентности элемента. О3 имеет несколько резонансных структур.
Методы синтеза
Для образования такого газа, как озон, химический элемент оксиген должен находиться в газообразной среде в виде отдельных атомов. Такие условия создаются при соударении молекул кислорода О2 с электронами во время электрических разрядов или другими частицами с большой энергией, а также при его облучении ультрафиолетом.
Львиная доля от общего количества озона в естественных условиях атмосферы образуется фотохимическим способом. Человек предпочитает в химической деятельности использовать другие методы, такие как, например, электролитический синтез. Он заключается в том, что в водную среду электролита помещают платиновые электроды и пускают ток. Схема реакции:
Физические свойства
Кислород (О) – составная единица такого вещества как озон — химический элемент, формула которого, а также относительная молярная масса указаны в таблице Менделеева. Образуя О3, оксиген приобретает свойства, кардинально отличающиеся от свойств О2.
Газ голубого цвета – это обычное состояние такого соединения, как озон. Химический элемент, формула, количественные характеристики — все это определили при идентификации и изучении данного вещества. Температура кипения для него -111,9 °C, сжиженное состояние имеет темно-фиолетовый окрас, при дальнейшем понижении градуса до -197,2 °C начинается плавление. В твёрдом агрегатном состоянии озон приобретает чёрный цвет с фиолетовым отливом. Растворимость его в десять раз превышает это свойство кислорода О2. При самых незначительных концентрациях в воздухе чувствуется запах озона, он резок, специфичен и напоминает запах металла.
Химические свойства
Очень активным, с реакционной точки зрения, является газ озон. Химический элемент, который его образует – это кислород. Характеристики, определяющие поведение озона во взаимодействии с другими веществами, – это высокая окисляющая способность и неустойчивость самого газа. При повышенных температурах он разлагается с небывалой скоростью, процесс ускоряют и катализаторы, такие как оксиды металлов, хлор, диоксид азота и другие. Свойства окислителя присущи озону благодаря особенностям строения молекулы и подвижности одного из атомов оксигена, который отщепляясь, превращает газ в кислород: О3 → О2 + О·
Оксиген (кирпичик, из которого построены молекулы таких веществ, как кислород и озон) – химический элемент. Как пишется в уравнениях реакции — О·. Озон окисляет все металлы, за исключением золота, платины и его подгруппы. Он реагирует с газами, находящимися в атмосфере – оксидами серы, азота и прочими. Не остаются инертными и органические вещества, особенно быстро идут процессы разрывов кратных связей через образования промежуточных соединений. Крайне важно, что продукты реакций являются безвредными для окружающей среды и человека. Это вода, кислород, высшие оксиды различных элементов, окислы углерода. Во взаимодействие с озоном не вступают бинарные соединения кальция, титана и кремния с кислородом.
Применение
Основная область, где применяется «пахнущий» газ – это озонирование. Подобный метод стерилизации гораздо эффективнее и безопаснее для живых организмов, чем дезинфекция хлором. При очищении воды озоном не происходит образование токсичных производных метана, замещенных опасным галогеном.
Всё чаще такой экологический метод стерилизации находит применение в пищевой отрасли промышленности. Озоном обрабатывают холодильное оборудование, складские помещения для продуктов, с помощь него проводят устранение запахов.
Для медицины дезинфицирующие свойства озона также незаменимы. Им обеззараживают раны, физиологические растворы. Озонируют венозную кровь, а также «пахнущим» газом лечат ряд хронических заболеваний.
Нахождение в природе и значение
Простое вещество озон – элемент газового состава стратосферы, области околоземного пространства, расположенной на расстоянии порядка 20-30 км от поверхности планеты. Выделение этого соединения происходит во время процессов, связанных с электрическими разрядами, при сварке, работе аппаратов ксерокса. Но именно в стратосфере образуется и содержит 99% от общего количества озона, находящегося в атмосфере Земли.
Жизненно важным оказалось присутствие газа в околоземном пространстве. Он образует в нем так называемый озоновый слой, который защищает всё живое от смертельного ультрафиолетового излучения Солнца. Как ни странно, но наравне с огромной пользой, сам газ опасен для людей. Повышение концентрации озона в воздухе, которым дышит человек, вредно для организма, вследствие его крайней химической активности.
Источник статьи: http://fb.ru/article/193500/ozon-himicheskiy-element-svoystva-formula-oboznachenie