Хлорид меди (I)
| Хлорид меди (I) | |
|---|---|
 | |
 | |
| Систематическое наименование | Хлорид меди (I) |
| Традиционные названия | Хлористая медь |
| Хим. формула | CuCl |
| Состояние | твёрдое |
| Молярная масса | 98,999 г/моль |
| Плотность | 4,145 г/см³ |
| Температура | |
| • плавления | 426 °C |
| • кипения | 1490 °C |
| Энтальпия | |
| • образования | -136 кДж/моль |
| Растворимость | |
| • в воде | 0,0062 г/100 мл |
| Показатель преломления | 1,930 |
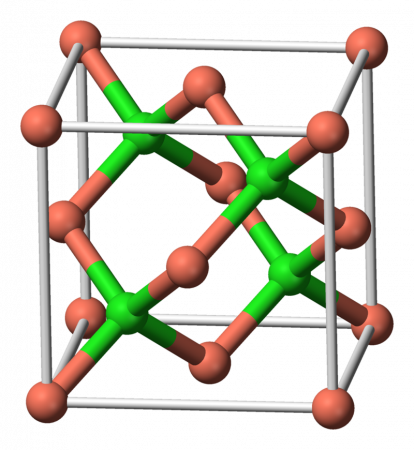
| Кристаллическая структура | Структура цинковой обманки |
| Рег. номер CAS | 7758-89-6 |
| PubChem | 62652 |
| Рег. номер EINECS | 231-842-9 |
| SMILES | |
| RTECS | GL6990000 |
| ChEBI | 53472 |
| Номер ООН | 2802 |
| ChemSpider | 56403 |
| ЛД50 | 140 мг/кг |
| Пиктограммы СГС |    |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Хлорид меди (I) — бинарное химическое соединение, медная соль хлороводородной кислоты.
Представляет собой белый или зеленоватый порошок, практически нерастворимый в воде (0,0062 г/100 мл при 20 °C). Зеленоватую окраску придают примеси хлорида меди (II).
Содержание
История открытия
Впервые хлорид меди (I) был получен Робертом Бойлем в 1666 году, из хлорида ртути (II) и металлической меди:
HgCl2 + 2Cu ⟶ 2CuCl + Hg
В 1799 году, Джозеф Луи Пруст успешно отделил дихлорид меди от монохлорида и описал эти соединения. Это было достигнуто путём нагревания CuCl2 в бескислородной среде, в результате чего хлорид меди(II) потерял половину связанного хлора. После этого он удалил остатки дихлорида меди от хлорида меди (I) и промыл водой.
Физические свойства
Монохлорид меди образует кристаллы белого цвета, кубической сингонии, пространственная группа F 4 3m, параметры ячейки a = 0,5418 нм , Z = 4 , структура типа ZnS. При нагревании кристаллы синеют. При температуре 408 °C CuCl переходит в модификацию гексагональной сингонии, пространственная группа P 63mc, параметры ячейки a = 0,391 нм , c = 0,642 нм , Z = 4 .
Монохлорид меди плавится и кипит без разложения. В пара́х молекулы полностью ассоциированы (димеры с незначительной примесью тримеров), поэтому формулу вещества иногда записывают как Cu2Cl2.
Плохо растворим в воде (0,062% при 20 °C), но хорошо в растворах хлоридов щелочных металлов и соляной кислоте. Так в насыщенном растворе NaCl растворимость CuCl составляет 8% при 40 °C и 15% при 90 °C. Водный раствор аммиака растворяет CuCl с образованием бесцветного комплексного соединения [Cu(NH3)2]Cl.
Получение
В природе монохлорид меди встречается в виде редкого минерала нантокит (по названию села Нантоко, Чили), который благодаря подмеси атакамита часто окрашен в зелёный цвет.
В промышленности монохлорид меди получают несколькими способами:
- Хлорирование избытка меди, взвешенной в расплавленном CuCl:
2Cu + Cl2 → 450oC 2CuCl
- Восстановление CuCl2 медью в подкисленном растворе:
Cu + CuCl 2 → 80oC,HCl 2 CuCl ↓
В лабораторной практике последний метод также широко распространён.
- Очень чистый препарат получается при взаимодействии меди с газообразным хлористым водородом:
2Cu + 2HCl → 500−600oC 2CuCl + H2
- Похожая реакция идёт в растворе в присутствии окислителей (O2, HNO3, KClO3):
4Cu + 4HCl + O2 → 70−80oC 4 CuCl + 2H2O
- Удобен способ восстановления меди (II) диоксидом серы:
2CuSO4 + 2NaCl + SO2 + 2H2O → 2 CuCl ↓ + 2H2SO4 + Na2SO4
- Восстановление сульфитом при избытке хлоридов:
2Cu 2+ + 3Cl − + 3SO3 2− + H2O → 2CuCl↓ + 2SO4 2− + 2HSO3 −
- Возможна реакция конпропорционирования:
CuSO4 + Cu + 2NaCl → 70oC,HCl 2 CuCl ↓ + Na2SO4
- Возможно получение монохлорида меди термическим разложением дихлорида:
2 CuCl 2 → ∼1000oC 2 CuCl + Cl2
Химические свойства
- При кипячении суспензии монохлорида меди происходит реакция диспропорционирования:
2 CuCl → 100oC CuCl 2 + Cu
- Монохлорид меди обратимо растворяется в соляной кислоте с образованием комплексного соединения:
CuCl + HCl ⇄ H[ CuCl 2]
- Монохлорид меди устойчив в сухом воздухе, но во влажном начинает окисляться до основного хлорида (который и придаёт кристаллам зелёный цвет):
4 CuCl + O2 + 2H2O → 4 CuCl (OH)
- В кислой среде окисление приводит к образованию нормальных солей:
4CuCl + 4HCl + O2 → 95oC 4 CuCl 2 + 2H2O
- Окисление можно проводить и горячей концентрированной азотной кислотой:
CuCl + 3HNO3 → τ Cu(NO3)2 + HCl + NO2↑ + H2O
- Аммиачные растворы монохлорида меди поглощают ацетилен с образованием красного осадка:
2 CuCl + C2H2 + 2NH3 → Cu2C2↓ + 2NH4Cl
- Кислые растворы монохлорида меди обратимо поглощают окись углерода:
CuCl + CO ⇄ CuCl ⋅ CO
Применение
- Монохлорид меди — промежуточный продукт при производстве меди.
- Поглотитель газов при очистке ацетилена, а также CO в газовом анализе.
- Катализатор в органическом синтезе, например при окислительном хлорировании метана или этилена, в производстве акрилонитрила.
- Антиоксидант для растворов целлюлозы.
Физиологическое действие
Хлорид меди (I) ядовит. Может привести к тяжёлым отравлениям. Относится ко 2-му классу опасности.
Источник статьи: http://chem.ru/hlorid-medi-i.html
Как пишется хлорид меди
Wikimedia Foundation . 2010 .
Смотреть что такое «Хлорид меди(II)» в других словарях:
Хлорид меди — неорганическое соединение меди с хлором. Известны следующие хлориды меди: Хлорид меди(I) CuCl; Хлорид меди(II) CuCl2 … Википедия
Хлорид меди(I) — У этого термина существуют и другие значения, см. Хлорид меди. Хлорид меди(I) … Википедия
хлорид меди(I) — хлористая медь(I) … Cловарь химических синонимов I
хлорид меди(II) — хлорная медь … Cловарь химических синонимов I
Хлорид — меди (I) Хлориды группа химических соединений, соли хлороводородной (соляной) кислоты HCl. Ионные хлориды твёрдые кристаллические вещества с высокими температурами плавления, проявляющие основные свойства; ковалентные газы, жидкости или… … Википедия
Хлорид брома — Хлорид брома … Википедия
Хлорид иттрия — Общие Систематическое наименование Хлорид иттрия Традиционные названия Хлористый иттрий Химическая формула YCl3 Физические свойства Состояние ( … Википедия
меди(II) хлорид — vario(II) chloridas statusas T sritis chemija formulė CuCl₂ atitikmenys: angl. copper dichloride; copper(II) chloride rus. меди дихлорид; меди(II) хлорид; медь двухлористая; медь хлорная ryšiai: sinonimas – vario dichloridas … Chemijos terminų aiškinamasis žodynas
меди(I) хлорид — vario(I) chloridas statusas T sritis chemija formulė Cu₂Cl₂ atitikmenys: angl. copper(I) chloride rus. меди(I) хлорид; медь хлористая ryšiai: sinonimas – divario dichloridas … Chemijos terminų aiškinamasis žodynas
Источник статьи: http://dic.academic.ru/dic.nsf/ruwiki/1343018

