Бромоводородная кислота как пишется
бромоводородная кислота — (HBr) [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность EN hydrogen bromide … Справочник технического переводчика
бромоводородная кислота — (бромистоводородная кислота), раствор бромоводорода в воде, одна из самых сильных кислот (сильнее, чем соляная кислота). Чистая бромоводородная кислота бесцветная, на воздухе буреет (медленно окисляется, выделяя бром). Сильный восстановитель.… … Энциклопедический словарь
БРОМОВОДОРОДНАЯ КИСЛОТА — (бромистово дородная кислота), р р бромоводорода в воде, одна из самых сильных к т (сильнее, чем соляная кислота). Чистая Б. к. бесцветная, на воздухе буреет (медленно окисляется, выделяя бром). Сильный восстановитель. Соли Б. к. бромиды. Б. к.… … Естествознание. Энциклопедический словарь
Кислота — У этого термина существуют и другие значения, см. Кислота (значения) … Википедия
бромистоводородная кислота — то же, что бромоводородная кислота … Энциклопедический словарь
БРОМИСТОВОДОРОДНАЯ КИСЛОТА — то же,что бромоводородная кислота … Естествознание. Энциклопедический словарь
Кислоты и ангидриды — Служебный список статей, созданный для координации работ по развитию темы. Данное предупреждение не устанавл … Википедия
Кислоты и ангидриды — КИСЛОТЫ И АНГИДРИДЫ. Кислоты класс химических соединений характеризующихся диссоциацией в водном растворе с образованием гидратированных ионов H+. Ангидриды химические соединения, производные органических и неорганических кислот, образующиеся при … Российская энциклопедия по охране труда
Кислоты — У этого термина существуют и другие значения: Кислота (наркотик) Кислоты один из основных классов химических соединений. Они получили своё название из за кислого вкуса большинства кислот, таких, как азотная или серная. По определению кислота … … Википедия
Источник статьи: http://dic.academic.ru/dic.nsf/ruwiki/822091
Бромоводородная кислота. Способы получения, физические и химические свойства
Бромоводородная кислота (другое название бромоводород) — это неорганическое соединение водорода (H) с бромом (Br). Это бесцветный газ, который во влажном воздухе образует густой туман.
Какие существуют способы получения бромоводорода
По причине высокой степени окисляемости бромоводороной кислоты, ее нельзя получить посредством воздействия серной кислоты концентрированной на бромиды металлов щелочных. Происходит следующая реакция:
2KBr (бромид калия) + 2Н2SO4 (кислота серная) = К2SO4 (калия сульфат) + SO2 (оксид серы) + Br2 (молекула брома) + 2Н2О (вода)
1. В промышленности получение кислот, таких как бромоводородная, осуществляется посредством реакции, в ходе которой взаимодействуют составляющие элементы. Например, рассматриваемое нами вещество можно получить следующим способом:
H2 (молекула водорода) + Br2 (молекула брома) = 2HBr (бромоводородная кислота)
Эта реакция осуществима при температуре от 200 до 400 градусов.
2. Также возможно получение бромоводородной кислоты и в лабораторных условиях несколькими способами.
— посредством гидролиза пентабромида фосфора или трибромида:
PBr3 (трибромид) + 3H2O (три молекулы воды) = H3PO3 (кислота фосфорная) + 3HBr (бромоводородная кислота, формула химическая)
PBr5 (пентабромид) + 4H2O (четыре молекулы воды) = H3PO4 (кислота фосфорная) + 5HBr (бромоводород)
— путем восстановления брома:
3Br2 (три молекулы брома) + S (сера) + 4H2O (вода) = (реакция возможна при температуре, равной 100-150 градусов) H2SO4 (серная кислота) + 6HBr (бромоводород)
3Br2 (три молекулы брома) + KNO2 (калия нитрит) + 4H2O (вода) = KNO3 (нитрат калия) + 2HBr (бромоводород)
— посредством вытеснения разбавленной кислотой щелочных металлов из бромидов:
KBr (бромистый калий) + H2SO4 (серная кислота) = KHSO4 (калия гидросульфат) + HBr (выделяется в виде газа)
3. Как побочный продукт бромистый водород можно получить при синтезе органических бромопроизводных соединений.
Физические свойства бромоводорода:
1. Бромоводородная кислота — это газ без цвета, имеющий неприятный и резкий запах. Сильно дымится на воздухе. Обладает высокой устойчивостью к температурам.
2. Хорошо растворяется в H2O (вода) и этаноле с образованием электролита. Водный раствор бромоводорода образует азеотропную смесь, которая кипит при температуре 124 градуса. В одном литре воды растворяется около полулитра бромводорода (при 0 градусов).
3. В процессе охлаждения водного раствора бромистого водорода можно получить следующие кристаллогидраты: HBr*H2O, HBr*2H2O, HBr*4H2O.
4. Чистый бромоводород образует кристаллы сингонии орторомбической, пространственной группы F mmm.
5. При температуре -66,8 градусов переходит в жидкое состояние, а при — 87 градусов затвердевает.
Химические свойства бромоводорода:
1. Бромоводородная кислота при взаимодействии с водой образует сильную кислоту одноосновную. Эта реакция выглядит так:
HBr + H2O (вода) = Br- (анион брома) + H3O+ (ион гидроксония)
2. Данное вещество устойчиво к высоким температурам, однако, при 1000 градусах около 0,5% всех молекул разлагаются:
2HBr (бромоводородная кислота) = H2 (молекула водорода) + Br2 (молекула брома)
3. Рассматриваемое нами химическое соединение реагирует с различными металлами, а также их основаниями и оксидами. Примеры реакций:
2HBr + Mg (магний) = MgBr2 (бромид магния) + H2 (выделяется в виде газа)
2HBr + CaO (кальция оксид) = CaBr2 (бромид кальция) + H2O (вода)
HBr + NaOH (натрия гидроксид) = NaBr (бромид натрия) + H2O (вода)
4. Бромоводород также является восстановителем. На воздухе медленно окисляется. По этой причине его водные растворы через некоторое время окрашиваются в бурый цвет. Реакция будет такая:
4HBr (бромоводородная кислота) + O2 (молекула кислорода) = 2Br2 (молекула брома) + 2H2O (вода)
Бромоводород используют для создания (синтеза) различных органических производных брома и для приготовления бромидов различных металлов. Особенное значение имеет бромид серебра, так как он используется в производстве кинофотоматериалов.
Как производится транспортировка
В баллонах емкостью 68 или 6,8 литров под давлением в 24 атмосферы.
Источник статьи: http://fb.ru/article/47093/bromovodorodnaya-kislota-sposobyi-polucheniya-fizicheskie-i-himicheskie-svoystva
Бромистоводородная кислота — опасный, но важный химический реактив
Бромистоводородная кислота — сильная неорганическая кислота, ее формула HBr. 
В промышленных масштабах вещество получают химической реакцией водорода и брома в процессе нагревания, а так же как побочный продукт органического синтеза бромосодержащих соединений.
Свойства
Бромоводород в нормальных условиях представляет собой газ тяжелее воздуха, без цвета, с кислым вкусом, очень гигроскопичный. Газ сильно «дымит» на воздухе, активно поглощая влагу и образуя туман — капельки водной кислоты. Запах резкий, неприятный, напоминает запах соляной кислоты. При температуре около -67 °С сгущается в жидкость, а при t -87 °С кристаллизируется. Может образовывать кристаллогидраты.
Кислота хорошо растворяется в воде, спиртовой раствор образует электролит. Термически устойчива, даже при нагревании до 1000 °С на водород и бром разлагается не более полпроцента молекул вещества.
Водный раствор HBr — прозрачная бесцветная или слегка желтоватая жидкость. Желтый цвет раствору придают молекулы Br, образующиеся в процессе реакции вещества с кислородом воздуха. Реактив тяжелее воды, с резким запахом. С точки зрения химии — это одноосновная кислота с восстановительными свойствами. Считается одной из самых сильных кислот, по своей активности сопоставима с соляной кислотой. Реагирует с металлами, оксидами и щелочами с образованием бромидов. В реакции с металлами выделяет водород, который может воспламениться. Бромистоводородная кислота разрушает большинство металлов. Ее смесь с азотной кислотой способна растворять золото и платину.
Меры безопасности

Гост 2062-77 требует, чтобы работы с бромоводородом велись с использованием средств защиты лица, глаз, тела, органов дыхания, в вытяжном шкафу, с учетом правил противопожарной безопасности. Для нейтрализации пролитого реактива используют 10% раствор щелочи или большое количество воды. Для осаждения паров разлитой кислоты разбрызгивают воду. Газ тяжелее воздуха, поэтому при аварийных выбросах скапливается в нижней части помещения, в подвалах, в низинах.
HBr допускается перевозить любым транспортом с соответствующей маркировкой тары знаком опасности по ГОСТ 19433. Газообразная кислота транспортируется в баллонах под давлением 24 атм. Наиболее подходящая тара для хранения водной кислоты — пластиковые канистры.
Применение
— Бромистоводородная кислота, ее газообразная форма и водные растворы разной 
— Реактив используется как катализатор в реакциях алкилирования в органическом синтезе.
— Бромоводород востребован в аналитической химии и микробиологии, в нефтяной и химической индустрии.
В интернет-магазине реактивов и химического оборудования «ПраймКемикалс Групп» можно купить как бромистоводородную кислоту, так и пластиковую и стеклянную тару для нее, а также средства защиты для работы с агрессивными веществами.
Источник статьи: http://pcgroup.ru/blog/bromistovodorodnaya-kislota-opasnyj-no-vazhnyj-himicheskij-reaktiv/
бромоводородная кислота
Энциклопедический словарь . 2009 .
Смотреть что такое «бромоводородная кислота» в других словарях:
бромоводородная кислота — (HBr) [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность EN hydrogen bromide … Справочник технического переводчика
Бромоводородная кислота — Бромоводород Общие Систематическое наименование бромоводород Химическая формула … Википедия
БРОМОВОДОРОДНАЯ КИСЛОТА — (бромистово дородная кислота), р р бромоводорода в воде, одна из самых сильных к т (сильнее, чем соляная кислота). Чистая Б. к. бесцветная, на воздухе буреет (медленно окисляется, выделяя бром). Сильный восстановитель. Соли Б. к. бромиды. Б. к.… … Естествознание. Энциклопедический словарь
Кислота — У этого термина существуют и другие значения, см. Кислота (значения) … Википедия
бромистоводородная кислота — то же, что бромоводородная кислота … Энциклопедический словарь
БРОМИСТОВОДОРОДНАЯ КИСЛОТА — то же,что бромоводородная кислота … Естествознание. Энциклопедический словарь
Кислоты и ангидриды — Служебный список статей, созданный для координации работ по развитию темы. Данное предупреждение не устанавл … Википедия
Кислоты и ангидриды — КИСЛОТЫ И АНГИДРИДЫ. Кислоты класс химических соединений характеризующихся диссоциацией в водном растворе с образованием гидратированных ионов H+. Ангидриды химические соединения, производные органических и неорганических кислот, образующиеся при … Российская энциклопедия по охране труда
Кислоты — У этого термина существуют и другие значения: Кислота (наркотик) Кислоты один из основных классов химических соединений. Они получили своё название из за кислого вкуса большинства кислот, таких, как азотная или серная. По определению кислота … … Википедия
Источник статьи: http://dic.academic.ru/dic.nsf/es/10036/%D0%B1%D1%80%D0%BE%D0%BC%D0%BE%D0%B2%D0%BE%D0%B4%D0%BE%D1%80%D0%BE%D0%B4%D0%BD%D0%B0%D1%8F
Формула бромоводородной кислоты
Определение и формула бромоводородной кислоты
Плотность – 3,6445 г/л (н.у.). Сильная кислота. Растворяется в этаноле (слабый электролит). Реагирует с концентрированной серной кислотой, щелочами, металлами, хлором. Медленно окисляется в кислороде. Проявляет окислительно-восстановительные свойства.
Химическая формула бромоводородной кислоты
Химическая формула бромоводородной кислоты HBr. Она показывает, что в состав данной молекулы входят один атом брома (Ar = 80 а.е.м.) и один атом водорода (Ar = 1 а.е.м.). По химической формуле можно вычислить молекулярную массу бромоводородной кислоты:
Графическая (структурная) формула бромоводородной кислоты
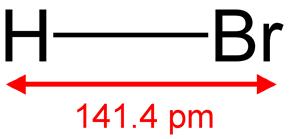
Структурная (графическая) формула бромоводородной кислоты является более наглядной. Она показывает то, как связаны атомы между собой внутри молекулы (рис. 1).
Рис. 1. Графическая формула бромоводородной кислоты.
Ионная формула
Бромоводородная кислота представляет собой электролит, который диссоциирует на ионы в водном растворе согласно следующему уравнению реакции:
Примеры решения задач
| Задание | Определите молекулярную формулу кальциевой селитры, в которой массовые отношения кальция, азота и кислорода равны 10:7:24. Относительная молекулярная масса кальциевой селитры 164. |
| Решение | Для того, чтобы узнать, в каких отношениях находятся химические элементы в составе молекулы необходимо найти их количество вещества. Известно, что для нахождения количества вещества следует использовать формулу: |
Найдем молярные массы кальция, азота и кислорода (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Известно, что M = Mr, значит M(Ca)= 40 г/моль, Ar(N)=14 г/моль, а М(O) = 32 г/моль.
Тогда, количество вещества этих элементов равно:
n(Ca) :n(N):n(O) = 0,25 : 0,5 : 1,5= 1 : 2 : 6,
т.е. простейшая формула соединения кальция, азота и кислорода имеет вид CaN2O6 и молярную массу 164 г/моль [M(CaN2O6) = Ar(Ca) + 2×Ar(N) + 6×Ar(O) = 40 + 2×14 + 6×16 = 40 + 28 + 96 = 164 г/моль]
Чтобы найти истинную формулу органического соединения найдем отношение полученных молярных масс:
Значит формула соединения кальция, азота и кислорода имеет вид CaN2O6или Ca(NO3)2. Это нитрат кальция.
| Задание | Установите массовую формулу вещества, содержащего 55,2% калия, 14,6% фосфора и 30,2% кислорода. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле: |
Обозначим количество моль элементов, входящих в состав соединения за «х» (калий), «у» (фосфор) и «z» (кислород). Тогда, мольное отношение будет выглядеть следующим образом (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел):
Значит формула соединения калия, фосфора и кислорода будет иметь вид K3PO4. Это фосфат калия.
Источник статьи: http://ru.solverbook.com/spravochnik/formuly-po-ximii/formula-bromovodorodnoj-kisloty/